
技术文章
Technical articles 热门搜索:
Fitzgerald Industries International代理
Envirologix 转基因快速检测试纸
Epitomics现货抗体目录
ABgene代理30
Cayman Chemical 特约代理
EVE™ Slide(EVE细胞计数板)
法国ID-VET
Sinobio公司产品介绍
美国Sutter 玻璃毛坯 BF100-50-10
Abcam代理
genview
D12079BWestern Diet(高纯度饲料)
TEAA Solution(货号:553303;SP5890)
LSPN-50ABMI公司LYSOSTAPHIN中国总代理
天然小鼠补体C1q蛋白
merck 2012年价格表
热门搜索:
Fitzgerald Industries International代理
Envirologix 转基因快速检测试纸
Epitomics现货抗体目录
ABgene代理30
Cayman Chemical 特约代理
EVE™ Slide(EVE细胞计数板)
法国ID-VET
Sinobio公司产品介绍
美国Sutter 玻璃毛坯 BF100-50-10
Abcam代理
genview
D12079BWestern Diet(高纯度饲料)
TEAA Solution(货号:553303;SP5890)
LSPN-50ABMI公司LYSOSTAPHIN中国总代理
天然小鼠补体C1q蛋白
merck 2012年价格表
 更新时间:2020-04-09
更新时间:2020-04-09 点击次数:2747
点击次数:2747
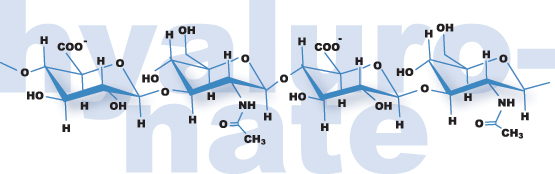
透明质酸钠医药级是一种高度纯化且特性良好的透明质酸钠,开发用于生物医学和制药应用。透明质酸钠药物级由日本NovaMatrix®战略合作伙伴Kikkoman Biochemifa Company(KBC)生产。超纯透明质酸钠的发酵基于10多年的经验,该工厂的建造和运行符合cGMP散装药品指南。来自基本的超纯透明质酸钠在提交给美国FDA的DMF中有所描述。除透明质酸钠外,NovaMatrix®还分别提供超纯藻酸盐和壳聚糖,聚阴离子和聚阳离子聚合物,可与透明质酸结合使用。
从兽疫链球菌发酵的透明质酸钠是一种线性共聚物,由(ß-1,4)连接的D-葡萄糖醛酸酯和(ß-1,3)-N-乙酰基-D-葡萄糖胺组成。透明质酸钠是一种丰富的糖胺聚糖,存在于所有高级动物的皮肤,关节,眼睛以及大多数器官和组织的细胞外基质中。它是仅有的非硫酸化糖胺聚糖,可形成高粘度水溶液。
粘度是聚合物膨胀的无规卷曲结构的直接结果,是强氢键合的结果。透明质酸盐的卷曲结构可以将其重量捕获约1000倍的水。这些特性赋予该分子*的物理化学特性以及*的生物学功能,并使其成为药物递送,组织工程和粘液补充中新型生物相容性和生物相互作用材料的有吸引力的构建基块。
透明质酸或透明质酸盐是哺乳动物有机体中的天然成分,并且会因透明质酸酶而发生聚合物链酶促降解。透明质酸盐在内皮组织中的半衰期少于一天,而成年人中该聚合物的自然周转率约为每天7g。乙酰透明质酸的轻度至中度共价修饰会增加体内稳定性和保留时间,从几天到几个月或一年不等。聚合物的生物力学性能也通过共价改性技术得到改善。目前的修饰主要集中在D和N单体单元上的羧基和羟基,以及聚合物交联技术。

透明质酸钠医药级是为生物医学和制药应用开发的高度纯化且特性良好的透明质酸钠。我们的透明质酸钠药物等级是由NovaMatrix®战略合作伙伴KBC按照适用的日本法律和GMP准则生产的;ICH Q7;和ISO标准:ISO 9001:2008和ISO 14001:2004。
透明质酸钠药物等级符合当前《欧洲药典》中规定的标准,并满足ASTM F2347中规定的用于组织工程医疗产品的要求。透明质酸钠药物等级在提交给美国FDA的DMF中有描述
透明质酸钠药物等级80
$78,00 / gram
SKU:产品#4266107
类别:超纯透明质酸钠
透明质酸钠医药级FCH 80是基于从兽疫链球菌发酵而得的透明质酸钠发酵并纯化*高的纯度。内毒素和蛋白质的残留水平可直接在体内使用,而无需在给药前进行任何变应原性测试。该产品的分子量在620000 – 1150000 g / mol范围内(根据特性粘度数据计算)。每克出售,低订购量为10克。
| 通用名 | 透明质酸钠 |
|---|---|
| 存储 | 存放在2-8°C的密闭容器中,避光和防潮 |
| 识别-红外光谱 | 在约3400 cm-1、2900 cm-1、1610 cm-1、1400 cm-1、1040 cm-1和610 cm-1处显示吸光度 |
| 鉴定-钠的反应 | 形成密集的白色沉淀 |
| 600 nm处的吸光度 | 不大于0.01 |
| 出现 | 清晰的解决方案 |
| pH值 | 5.5 – 8.5(0.5%水溶液) |
| 特性粘度 | 1.2 – 2.0立方米/千克 |
| 核酸(260nm处的吸光度) | 不大于0.2 |
| 蛋白 | 不超过0.1% |
| 乙醇 | 不超过1.0% |
| 重金属 | 不超过10ppm |
| 氯化物 | 不超过0.5% |
| 铁 | 不超过80ppm |
| 干燥失重 | 不超过10.0% |
| 微生物污染(生物负荷) | 不超过20 cfu / g |
| 细菌内毒素 | 不超过2.5 EU / g |
| 含量 | 95.0 – 105.0% |
NovaMatrix®生产并提供用于制药,生物技术和生物医学行业的,特征明确且有据可查的超纯,生物相容性和生物可吸收性生物聚合物。
这些可能包括但不限于诸如药物输送,组织工程,细胞封装和医疗设备之类的应用。对于我们的超纯藻酸钠和透明质酸钠,我们与美国FDA维护药物主文件。
NovaMatrix®产品旨在用于需要由我们的制造,质量控制和质量保证提供高质量和一致质量的应用中。NovaMatrix®在我们位于挪威的工厂中生产PRONOVA™海藻酸钠。我们按照GMP准则运作;ICH Q7,ICH Q1,ICH Q2和ISO标准;ISO 9001:2008和ISO 13485:2003。
此外,NovaMatrix®还拥有由挪威医学局(NOMA)颁发的API制造许可证。我们的透明质酸钠超纯产品是由我们的合作伙伴日本龟甲万生物化学公司根据GMP准则使用非动物来源生产的;《药品和医疗器械法案》,ICH Q7和ISO标准;ISO 9001:2008和ISO 14001:2004。
透明质酸钠医药级150
$78,00 / gram
KU:产品#4266206
类别:超纯透明质酸钠
透明质酸钠药物等级150是基于从兽疫链球菌发酵而得的透明质酸钠发酵并纯化*高的纯度。内毒素和蛋白质的残留水平可直接在体内使用,而无需在给药前进行任何变应原性测试。该产品的分子量在1400000 – 1800000 g / mol范围内(根据特性粘度数据计算)。每克出售,低订购量为10克。
| 通用名 | 透明质酸钠 |
|---|---|
| 存储 | 存放在2-8°C的密闭容器中,避光和防潮 |
| 识别-红外光谱 | 在约3400 cm-1、2900 cm-1、1610 cm-1、1400 cm-1、1040 cm-1和610 cm-1处显示吸光度 |
| 鉴定-钠的反应 | 形成密集的白色沉淀 |
| 溶液外观 | 清晰的解决方案 |
| 600 nm处的吸光度 | 不大于0.01 |
| pH值 | 5.3 – 6.8 |
| 特性粘度 | 2.1 – 2.8立方米/千克 |
| 核酸(260nm处的吸光度) | 不大于0.2 |
| 蛋白 | 不超过0.1% |
| 乙醇 | 不超过1.0% |
| 重金属 | 不超过20ppm |
| 氯化物 | 不超过0.5% |
| 铁 | 不超过80ppm |
| 干燥失重 | 不超过10.0% |
| 微生物*(生物负荷) | 不超过20 cfu / g |
| 细菌内毒素 | 不超过40 EU / g |
| 含量 | 95.0 – 105.0% |
NovaMatrix®生产并提供用于制药,生物技术和生物医学行业的,特征明确且有据可查的超纯,生物相容性和生物可吸收性生物聚合物。
这些可能包括但不限于诸如药物输送,组织工程,细胞封装和医疗设备之类的应用。对于我们的超纯藻酸钠和透明质酸钠,我们与美国FDA维护药物主文件。NovaMatrix®产品旨在用于需要我们制造商提供的高品质和一致质量的应用中,
质量控制和质量保证。NovaMatrix®在我们位于挪威的工厂中生产PRONOVA™海藻酸钠。我们按照GMP准则运作;ICH Q7,ICH Q1,ICH Q2和ISO标准;ISO 9001:2008和ISO 13485:2003。
此外,NovaMatrix®还拥有由挪威医学局(NOMA)颁发的API制造许可证。我们的透明质酸钠超纯产品是由我们的合作伙伴日本龟甲万生物化学公司根据GMP准则使用非动物来源生产的;《药品和医疗器械法案》,ICH Q7和ISO标准;ISO 9001:2008和ISO 14001:2004。